Khối lượng C 2 H 4 cần dùng để điều chế 2,5 tấn PE là bao nhiêu? biết hiệu suất quá trình điều chế đạt 80%
A. 3,125 tấn.
B. 3,215 tấn.
C. 2,0 tấn.
D. 3,512 tấn.
Khối lượng C 2 H 4 cần dùng để điều chế 2,5 tấn PE là bao nhiêu? biết hiệu suất quá trình điều chế đạt 80%
A. 3,125 tấn.
B. 3,215 tấn.
C. 2,0 tấn.
D. 3,512 tấn.
Từ 10 tấn NH3 sản xuất được bao nhiêu tấn dung dịch HNO3 biết hiệu suất của phản ứng điều chế HNO3 là 80% A.10 tấn. B.37,05 tấn. C.20 tấn. D.29,65 tấn
ý D
nNH3=10/17(mol)
NH3 + 2O2→nHNO3+H2O
10/17 →10/17
⇒mHNO3=10/17.63.80%=29,65 tấn
Để điều chế 1 tấn mỗi loại polime trên cần bao nhiêu tấn polime mỗi loại, biết rằng hiệu suất của hai phản ứng trên là 90%.
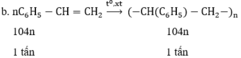
Khối lượng stiren cần dùng là m = 1 tấn
Vì H = 90% nên m = 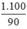 = 1,1(tấn )
= 1,1(tấn )
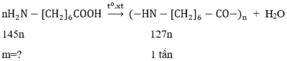
Khối lượng của axit ω-aminoentantic cần dùng là m = 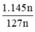 = 1,14 (tấn)
= 1,14 (tấn)
vì H = 90% nên m = 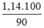 = 1,27(tấn )
= 1,27(tấn )
Từ 4 tấn C2H4 có chứa 20% tạp chất có thể điều chế bao nhiêu tấn PE ? (Biết hiệu suất phản ứng là 80%)
Để có 1 tấn thép (98% Fe) cần dùng bao nhiêu tấn quặng hematit nâu ( Fe 2 O 3 . 2 H 2 O ) ? Hàm lượng hematit nâu trong quặng là 80%. Hiệu suất quá trình phản ứng là 93%.
Khối lượng Fe: 1x98/100 = 0,98 tấn
Trong 196 tấn ( Fe 2 O 3 . 2 H 2 O ) có 112 tấn Fe
Trong 0,98 tấn Fe có 1,715 tấn ( Fe 2 O 3 . 2 H 2 O )
Khối lượng quặng : 1,715 x 100/80 = 2,144 tấn
Khối lượng quặng thực tế cần dùng: 2,144 x 100/93 = 2,305 tấn
Để sản xuất 1000 tấn gang chứa 95% Fe, 5% C ( các nguyên tố khác coi như không kể) thì phải dùng bao nhiêu tấn Fe2O3 và bao nhiêu tấn than cốc( C) ? biết hiệu suất của cả quá trình phản ứng là 80 %?
Giải thích các bước giải:
khối lượng của Fe và C trong 1000 tấn gang lần lượt là 950 tấn và 5 tấn
Vì hiệu xuất đạt 80 phần trăm => khối lượng Fe và C cần dùng lần lượt là 187,5 tấn và 6,25 tấn
Người ta điều chế Al từ một quặng có chứa 50% Al2O3. Biết hiệu suất phản ứng đạt 80%. Khối lượng Al thu được từ 2,04 tấn quặng trên là bao nhiêu tấn?
mAl2O3 =2,04.50% = 1,02 tấn
⇒ nAl2O3 = \(\frac{1,02}{102}\).106 = 0,01.106 mol
PTHH :
2Al2O3 --to,xt--> 4Al + 3O2
Theo PT trên nAl = 2nAl2O3 = 0,02.106 mol
⇒ nAl thu được = 0,02.106 .80% = 0,016.106 mol
⇒ mAl = 0,016.106 .27 = 0,432 .106 gam = 0,432 tấn
2Al2O3−→−−criolitđpnc4Al+3O2
mAl2O3=1,02(tan)=1020000(g)
⇒nAl2O3=10000(mol)
Theo pt: nAl=1/2nAl2O3=5000(mol)
⇒mAl(LT)=51000(g)=510(kg)
Mà: H% = 80%
⇒mAl(tt)=408(kg)
Từ 4 tấn C 2 H 4 có chứa 30% tạp chất có thể điều chế bao nhiêu tấn PE ? (Biết hiệu suất phản ứng là 90%)
A. 2,55
B. 2,8
C. 2,52
D. 3,6
Đáp án C
Bảo toàn khối lượng:
m PE = m Etilen pư = 4.0,7.90% = 2,52 tấn
Từ 4 tấn C 2 H 4 có chứa 30% tạp chất có thể điều chế bao nhiêu tấn PE? (Biết hiệu suất phản ứng là 90%)
A. 2,55
B. 2,8
C. 2,52
D. 3,6
Người ta điều chế Al từ một loại quặng có chứa 80% Al2 O3 . Biết hiệu suất của phản ứng đạt 75%. Khối lượng quặng để điều chế ra 5,4 tấn nhôm là
\(PTHH:2Al_2O_3\rightarrow4Al+3O_2\)
Cứ \(204\)tấn\(Al_2O_3\)tham gia pứ thì thu được \(108\) tấn \(Al\)
\(\Rightarrow\)Để thu được \(5,4\) tấn \(Al\) cần \(10,2\)tấn \(Al_2O_3\)
Vì: \(H=75\%\Rightarrow m_{Al_2O_3}=\frac{10,2.100}{75}=13,6\)(Tấn)
Mà quặng chỉ chứa\(80\%Al_2O_3\)
\(\Rightarrow\) Khối lượng quặng để điều chế\(5,4\)tấn \(Al\) là:
\(m_{quặng}=\frac{13,6.100}{80}=17\)(Tấn)
Vậy ......